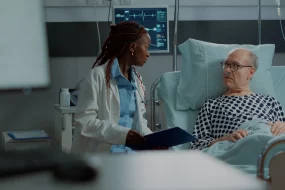
Primeira manhã do Congresso dirigido ao cuidado neurocrítico reuniu apresentações sobre o manejo e prognósticos de traumatismo cranioencefálico e parada cardiorrespiratória
No IV Congresso Internacional de Neurointensivismo, realizado no Rio de Janeiro entre os dias 3 e 6 de agosto de 2022, reuniram-se especialistas brasileiros e estrangeiros para discutir o estado da arte em diversas áreas da medicina intensiva neurocrítica. “O objetivo principal do congresso, que já se encontra na quarta edição, é trazer médicos de diferentes áreas para um mesmo evento, já que nós tratamos dos mesmos pacientes. Neurologistas, intensivistas e neurocirurgiões se reúnem em um fórum comum discutindo o tratamento e o diagnóstico de pacientes neurológicos críticos”, afirmou Pedro Kurtz, presidente da Associação Brasileira de Neurointensivismo e médico supervisor da UTI Neurológica do Instituto Estadual do Cérebro Paulo Niemeyer.
Segundo Kurtz, há uma série de novidades nessa edição do congresso, mas ele destaca os avanços no tratamento do acidente vascular cerebral isquêmico, que mudou muito nos últimos anos, com conquistas importantes dos grupos de pesquisa do Brasil. Uma delas foi a demonstração do benefício da trombectomia mecânica no tratamento desses pacientes. Kurtz destaca também os avanços obtidos em áreas como o traumatismo craniano grave, o acidente vascular cerebral hemorrágico e os pacientes pós-parada cardíaca, nas quais várias evidências vêm mostrando melhora nos desfechos com novos tratamentos.
“É preciso melhorar muito ainda em algumas áreas, principalmente na pesquisa clínica dentro da nossa realidade brasileira para entendermos se os tratamentos que funcionam lá fora funcionam também aqui e atuar muito em pesquisa de implementação, no que nós sabemos que funciona e ainda não é aplicado nos centros de tratamento intensivo brasileiros. Conseguir colocar em prática procedimentos que nós sabemos que funcionam é fundamental também”, afirmou Kurtz.
Manejo do Traumatismo Cranioencefálico
A primeira sessão temática do Congresso, na manhã do dia 5 de agosto, foi dedicada ao manejo do trauma cranioencefálico moderado a grave. Nela, Ricardo Turon, supervisor do Instituto do Cérebro Paulo Niemeyer e coordenador do Centro de Terapia Intensivo do Hospital Niterói D’Or, chamou atenção para a necessidade de desmistificar o fato de que a lesão axonal difusa seja, na sua totalidade, uma ruptura do axônio. Isso pode acontecer, mas não é o principal mecanismo. “Na verdade, a ruptura primária do axônio pós-trauma é relativamente rara. O que acontece é uma ruptura secundária após a deflagração de um processo inflamatório, que leva a uma interrupção da movimentação de proteínas e a um acúmulo de certas proteínas no axônio evidenciando os padrões histopatológicos observados”, apontou Turon.
Segundo Turon, a principal apresentação clínica na fase aguda é o coma, mas também fazem parte do espectro clínico alterações de memória, alterações de atenção e alterações das funções executivas superiores, que se observam em um momento posterior. “Essa apresentação clínica está relacionada com a lesão de sistemas integrados intrínsecos de axônios”, disse o médico. Uma pesquisa relativamente recente mostra que, quando a salience network, que inclui a insula anterior, o córtex cingulado anterior e o estriado ventral, e a deep neural network (DNN) são lesadas, ocorrem uma alteração do nível de consciência, uma alteração da atenção e uma alteração cognitiva das funções executivas superiores. “Pode-se observar que é nessas redes axonais que acontece a lesão axonal difusa”, afirmou Turon.
De acordo com o médico, há diversas perguntas que se fazem em relação aos pacientes com lesão axonal difusa. Como se faz a monitorização? O paciente desenvolve hipertensão intracraniana? É preciso colocar o cateter de pressão intracraniana (PIC)? Apesar de alguns estudos científicos terem mostrado que não há uma associação clássica da hipertensão intracraniana com a lesão axonal difusa, sabe-se que isso pode acontecer. Fazendo uma revisão sobre esses trabalhos, pode-se observar que alguns afirmam que a monitorização da pressão intracraniana é importante para a redução da mortalidade desses pacientes, enquanto outros mostram que esse procedimento não muda a mortalidade. “Minha opinião pessoal sobre isso é que, no caso de trauma cranioencefálico (TCE) grave, nós devemos monitorizar. É melhor pecar por excesso”, ponderou Turon.
Nos casos de TCE grave com perda de consciência e lesão axonal difusa pura, ele colocaria pelo menos um cateter de pressão intracraniana intraparenquimatoso por 48 horas, procedimento que não traz risco de infecção. Faria também um eletroencefalograma se o paciente se mantiver inconsciente por mais 24 horas, além de neuromonitorização, neurochat e neuroimagem repetida. “E, se tivesse acesso, faria microdiálise e PTIO2 (tensão de oxigênio do tecido). No entanto, não há uma evidência que nos obrigue a fazer isso”, disse o médico.
A monitorização se torna ainda mais relevante levando em consideração o fato de que para essa condição não existe um tratamento específico. “Há várias tentativas, estabilização de citoesqueleto, taxol, homeostático-iônico, bloqueadores dos canais de cálcio para diminuir a sobrecarga de cálcio intracelular, inibidores de protease, proteção mitocondrial, ciclosporina A. Vários artigos falam disso, mas não há uma conclusão em relação a esses trabalhos”.
Desfechos em pacientes com TCE
Por sua vez, Wellingson Paiva, professor livre-docente em Neurologia da Faculdade de Medicina da Universidade de São Paulo, onde atua como diretor do Laboratório de Fisiopatologia Neurocirúrgica, e coordenador do Departamento de Trauma da Sociedade Brasileira de Neurointensivismo, considerado um dos maiores pesquisadores em Neurocirurgia do Brasil, tratou em sua apresentação dos desfechos em pacientes com trauma encefálico grave na América Latina. Segundo Paiva, é inquestionável a relevância do traumatismo cranionencefálico (TCE), que apresenta tanto uma morbidade quanto uma mortalidade muito alta, ficando atrás somente do acidente vascular cerebral (AVC) em termos de morbidade.
No entanto, no Brasil e na América Latina como um todo os dados existentes são escassos e imprecisos. E esse é um grande problema. Enquanto no caso do AVC pode-se extrapolar as informações que vêm da Europa e dos Estados Unidos, quando se trata de TCE os mecanismos de trauma e a qualidade da assistência são diferentes, então o que se tem são pacientes distintos, com diferentes perfis de tratamento. “Isso faz com que nós precisemos obrigatoriamente conhecer nossos pacientes com traumatismo cranioencefálico no Brasil e na América Latina para predizer o prognóstico”, disse Paiva.
Na América Latina, as realidades, as adversidades e as dificuldades encontradas no tratamento dessas condições são semelhantes, havendo regiões ou estados onde a estrutura é melhor. Mesmo nos Estados Unidos, um estudo sobre a mortalidade por TCE mostrou que a região do meio-oeste, por exemplo, que tem menos estrutura, tem uma mortalidade extremamente alta, o que não se observa na costa leste, onde o serviço de saúde é mais preparado.
Segundo Paiva, é preciso pensar em um atendimento ao trauma que seja completo, o que esbarra em dificuldades. “A qualidade do pré-hospitalar aumentou muito nos grandes centros nos últimos anos, a padronização do atendimento na sala de emergência, a qualidade da UTI com o deslocamento da percepção do intensivista no sentido de deixar de ser um intensivista cardiopulmonar e entender que ele também deve ter conhecimento de neurointensivismo, isso melhorou bastante”, ponderou Paiva. Mas a maior dificuldade em sua opinião reside na reabilitação. “A reabilitação para o AVC melhorou muito, o cenário para uma lesão raquiomedular tem melhorado muito, até porque são pacientes que fazem um trabalho de cobrar as autoridades. Já a reabilitação para traumas de crânio, pelo fato de que a maioria dos pacientes tem uma perda cognitiva, tem sido muito limitado no Brasil e na América Latina quando comparadas com outros centros”.
No que concerne aos desfechos, Paiva aponta a necessidade de criar modelos prognósticos adequados à nossa realidade, sobretudo porque não há recursos para tratar todos os pacientes. Assim, é necessário entender quais são os pacientes que têm melhores chances a fim de definir estratégias de tratamento capazes de fazê-los retornar a suas famílias e retomar suas atividades. “Então, quando a gente pensa no prognóstico, a gente está pensando basicamente em recuperação funcional, morte e limitações neurológicas. E a gente precisa ter uma bola de cristal e olhar para esse paciente que está chegando na UTI e pensar como ele vai estar daqui a seis meses, daqui a um ano”, disse Paiva.
Os dois principais modelos conhecidos são o IMPACT (The International Mission for Prognosis and Analysis of Clinical Trials) e o CRASH (The Corticosteroid Randomization After Significant Head Injury), que criaram calculadoras para definir prognóstico. Mas também existem modelos baseados em neuroimagem, como o modelo tomográfico com classificação de Marshall, que tem uma correlação com o prognóstico em termos de recuperação funcional. “O paciente com Marshall 1 é bem diferente da evolução de um paciente com Marshall 4 ou Marshall 6, mostrando que é possível utilizar a tomografia também como um parâmetro”, explicou Paiva. Há ainda os escores de Rotterdam, publicado pelo prof. Maas, que leva em consideração critérios de neuroimagem, e de Helsinki, que é menos divulgado.
A construção de um modelo de prognóstico brasileiro
Levando em consideração os modelos existentes, Paiva e colegas buscaram construir um modelo aqui no Brasil baseado em um banco de dados com pacientes com traumatismo cranioencefálico leve ou moderado. “Quando nós fizemos a primeira avaliação nós tínhamos algo em torno de 500 pacientes, hoje nós estamos chegando a 1000 pacientes com TCE, e aí fizemos essa construção chegando a algumas informações em termos de curto prazo, como uma mortalidade de 27% para TCE grave”, explicou.
Comparando esse cenário de mortalidade com o que existe na literatura médica, Paiva e seus colaboradores fizeram diversas análises em termos de desfecho e chegaram aos principais critérios. Então eles fizeram algumas publicações baseadas nessas comparações, que possibilitaram aperfeiçoar os resultados encontrados na literatura. “Em um artigo publicado no ano passado, nós fizemos uma comparação para tentar melhorar a calculadora CRASH. Nós fizemos uma incorporação de informações sobre a coagulopatia, utilizando o TTPA (tempo de tromboplastina parcial ativado), uma informação relativamente simples, para tentar aperfeiçoar, criando um CRASH adaptado e obtendo um aumento da sensibilidade e da especificidade desse modelo”, apontou Paiva.
Quanto aos achados tomográficos, o grupo de Paiva publicou também no ano passado um estudo com um pouco mais de 200 pacientes analisando para validar uma informação importante, que é o desvio de linha média dos hematomas subdurais agudos, uma informação publicada em 1996. “Mostramos que o desfecho é muito pior nos pacientes que apresentam mais de 3 mm de diferença entre o hematoma subdural agudo e o desvio da estrutura da linha média”, afirmou Paiva. Em relação aos escores tomográficos, seu grupo fez uma análise para comparar os que existem para descobrir qual seria mais adequado para os pacientes brasileiros. “E a gente observou que a classificação de Marshall, a mais divulgada, é a que tem a menor acurácia em termos de predizer o prognóstico quando comparada com as outras duas, particularmente a de Rotterdam, que é mais utilizada, embora a de Helsinki tenha uma acurácia melhor, mas teoricamente o Marshall tem mais limitações, embora a gente utilize bastante no dia a dia com essa população”.
Além disso, o grupo de Paiva procurou utilizar processamentos estatísticos mais complexos, como machine learning, para condensar informações e obter variáveis que efetivamente modifiquem o prognóstico. “Há dois anos nós publicamos um trabalho em que utilizamos o machine learning para tentar identificar, em uma população com mais de 500 pacientes, utilizando um modelo linear, quais seriam essas variáveis. E aí são variáveis que são conhecidas de todos nós como tendo relação com o mau prognóstico, mas a gente precisava avaliar isso para ter certeza de que a nossa população tinha esse comportamento com relação ao que mostram outros estudos”, relembrou Paiva.
Outro grande problema nessa área são os desfechos tardios, porque é difícil seguir os pacientes em longo prazo. Eles de maneira geral são do Sistema Único de Saúde (SUS) e têm condições socioeconômicas limitadas, o que dificulta fazer o follow up. “Uma publicação desta semana de uma enfermeira do nosso grupo, a professora Rita, fez uma análise com pacientes com 12 meses e 24 meses. Nós verificamos que a nossa mortalidade depois que o paciente tem alta não é tão grande, mesmo um ano depois, dois anos depois, mas a recuperação funcional fica aquém do esperado em termos de bom resultado comparado com resultados encontrados na literatura. Talvez o fato de nosso suporte pós-alta do paciente não ser tão bom, com uma reabilitação ainda carente, seja uma das variáveis que explicam por que nossos dados são piores do que o que se encontra na literatura”, avaliou Paiva.
Outra possibilidade é utilizar modelos de neuroimagem avançada. “Então nós publicamos este ano um trabalho no qual analisamos algumas variáveis de neuroimagem com tensor de difusão em uma população com pouco mais de 60 pacientes. Temos dificuldade de fazer isso com um grupo maior, porque os custos são altos. Então fizemos essa amostra com um grupo pequeno, que foi submetido à neuroimagem, mostrando que alterações específicas do corpo caloso têm correlação com o grau de recuperação funcional desses pacientes. Nós também publicamos outro trabalho em que analisamos as alterações psiquiátricas e as alterações no corpo caloso, mostrando particularmente que o rosto do corpo caloso tem uma relação muito interessante em termos de capacidade de menores sintomas neuropsiquiátricos, particularmente transtorno de ansiedade e depressão”, afirmou.
Existe ainda a possibilidade de usar neuroimagem com modelo longitudinal. “Em um estudo do nosso grupo, nós utilizamos ressonância magnética com 3 meses, com 6 meses e um ano para observar a volumetria do córtex e o número de lesões. Não encontramos correlação entre o número de lesões e o desfecho dos pacientes, mas a volumetria cortical, quando a gente mede a espessura do córtex cerebral desses pacientes, quanto maior a perda – e isso é intuitivo, o que a gente fez foi documentar essas informações –, quanto mais atrofia cerebral se observa, piores são os desfechos cognitivos tanto de funções executivas quanto de memória desses pacientes”, ponderou.
Para alterar a realidade dos pacientes com trauma encefálico grave, na qual morre muita gente e muitas pessoas sofrem sequelas permanentes, Paiva propõe a uniformização do atendimento e da assistência que eles recebem, algo a ser feito na América Latina como um todo, onde é preciso seguir procedimentos que já foram experimentados com sucesso em outros lugares do mundo, com uma soma de esforços que envolvam o atendimento pré-hospitalar, a cirurgia de emergência, a neurocirurgia e a UTI, que precisam ser integrados.
Parada cardiorrespiratória e prognósticos
Gisele Sampaio, professora livre-docente da disciplina de Neurologia Clínica da Universidade Federal de São Paulo, pesquisadora do Hospital Israelita Albert Einstein e uma das organizadoras do congresso, em sua apresentação sobre a necessidade de evitar profecias autorrealizadas no manejo de pacientes pós-parada cardiorrespiratória e do estudo SPARE, que está começando. As profecias autorrealizadas têm relação com o prognóstico: quanto o resultado previsto para um paciente interfere nesse mesmo resultado? Quando um médico diz que o prognóstico é ruim, ele de fato pode ser ruim porque nada é feito para salvar o paciente. Esse é um grande problema nos estudos neurocríticos. “Por isso estamos tentando evitar isso criando modelos mais palpáveis, usando dados baseados em registros clínicos rigorosos para responder essa pergunta”, pontuou Sampaio.
Fazer a prognosticação não é uma tarefa simples. É preciso prever se o paciente vai ficar bem e quão bem ele vai ficar para informar o indivíduo ou sua família, que às vezes têm de tomar decisões difíceis, como a retirada de cuidados intensivos. “Na maioria das vezes, o paciente neurológico é um paciente que estava bem em casa, não estava esperando que acontecesse nada e não tem muito tempo para se preparar, para conversar com sua família sobre prognóstico. E por isso a gente fala tanto de modelos”, ponderou Sampaio.
Existem diversos modelos na terapia intensiva neurológica em que o médico pode se basear para fazer o prognóstico. Esses modelos matemáticos usualmente são desenvolvidos, em sua maioria, em populações com estudos retrospectivos e são validados de maneira prospectiva, posteriormente. A partir deles, os médicos tentam definir um cut put para aplicar os modelos nos pacientes individuais. “Uma das perguntas que fazemos é se os modelos que criamos para populações de pacientes são aplicáveis para aquele paciente individual”, disse Sampaio. É preciso considerar que para cada doença existe um mecanismo diferente de lesão: trauma é diferente de parada cardíaca, que é diferente do AVC isquêmico, que é diferente do AVC hemorrágico, por exemplo.
Segundo a médica, também é preciso levar em consideração que, ao conversar com o indivíduo acometido ou com sua família, os médicos transmitem informações como porcentagens relativas ao risco de o paciente ficar funcional ou não, mas o que a família ou o paciente pensam no momento de fazer sua decisão se baseia em aspectos que não são incluídos nos modelos prognósticos. “E isso tem um impacto grande na retirada de cuidado”, afirmou Sampaio. Em relação aos Estados Unidos, existe uma diferença cultural muito intensa. Aqui no Brasil, apenas 6% das decisões quanto à retirada de cuidados intensivos dependem do que os médicos apresentam às famílias, enquanto nos Estados Unidos essa frequência pode chegar a 30, 40 ou até 50%. “Então, as famílias levam muito em consideração a característica do que o paciente era anteriormente, e não só as porcentagens que a gente apresenta”, afirmou Sampaio.
Um estudo publicado em 2010 sobre a acurácia de neurointensivistas na previsão de prognósticos em uma unidade neurocrítica pós-parada cardiorrespiratória mostrou que em 80% dos casos esses profissionais acertaram. Entretanto, constatou-se que eles erravam mais quando previam um bom prognóstico do que ao prever um mau prognóstico. “Então, possivelmente quando a gente vê uma tomografia muito ruim, já cheia de lesões, a gente consegue com uma acurácia boa prever quem vai mal, mas não consegue prever que paciente vai estar funcional em longo prazo. E isso é um grande problema”, afirmou Sampaio. Com isso, os médicos se perguntam se estão fazendo o prognóstico de maneira correta.
Além disso, os modelos de prognosticação podem ter várias definições. “Por exemplo, eu posso tentar, do ponto de vista da saúde pública, entender qual é a porcentagem de leitos de UTI que eu preciso ter ou de neurorreabilitação que eu preciso ter então para isso o dado populacional é superútil”, ponderou Sampaio. Mas o modelo também pode ser construído para saber se uma intervenção está mudando ou não o prognóstico ou para balancear o estudo clínico com a inclusão de pacientes semelhantes. Assim, a própria função de prognosticar pode ser bastante diferente. No entanto, é preciso ter ferramentas para discutir prognóstico com os pacientes de forma individual.
Para responder as perguntas que se fazem os médicos quanto à certeza dos prognósticos, está se iniciando o estudo SPARE, um estudo observacional (sem intervenção), prospectivo, multicêntrico e internacional, que vai incluir pacientes do Brasil e dos Estados Unidos e vai durar bastante tempo. O objetivo é determinar o quanto o processo de retirada de cuidados intensivos influencia o prognóstico final que os médicos fazem para seus pacientes. “Então a gente vai incluir pacientes pós-parada cardiorrespiratória que estejam em coma nos dois países e acompanhar de uma maneira multimodal, avaliando de uma maneira prospectiva, não só com exame neurológico como também com vários marcadores de neuroimagem e eletroencefalografia”, explicou Sampaio. A ideia é garantir que a avaliação dos desfechos e a avaliação para fazer o prognóstico dos pacientes pelo médico à beira-leito serão feitas de uma maneira sistematizada para evitar os vieses e os erros que acontecem nos estudos retrospectivos e de registro.